快速掌握外泌體應用要點,降低誤區、提升研究與實務效益
- 蒐集近一年內5篇以上權威期刊或官方機構關於外泌體安全性與應用文獻
同步最新科學進展,避免落入過時或錯誤資訊陷阱
- 記錄所有相關副作用案例並定期(每6個月)交由專業醫療團隊評估
提早辨識潛在風險,有助優化使用流程和保障受試者安全
- 操作過程全程參考官方指引並預留10%以上資源進行品質控管與純化技術優化
確保外泌體穩定度及功能完整,減少失效率
- *每年至少一次*向細胞治療認證單位諮詢規範調整和新興應用動態
*緊貼產業法規變動,不因違規影響研發長遠佈局*
你對外泌體一頭霧水嗎?其實很多人跟你一樣困惑
你有沒有想過,身體裡那些微小的“快遞員”實際上正在影響你的健康決策?外泌體,這些直徑僅30至150納米的微小囊泡,正默默地在細胞間傳遞訊息。不少科學家認為它們可能是未來診斷和治療的新星,但許多人卻對它們仍感到陌生。別小看這個改變,它或許正在悄悄影響你的未來。但這麼多人都沒發現,背後原因可能沒你想得那麼簡單……
某生技公司投入外泌體研究,卻意外踩到這些地雷
在生物醫學研究中,外泌體的潛力引起了廣泛關注。根據最新報告,約有75%的科學家認為外泌體可以成為治療癌症的重要工具。然而,在實際應用中,一些團隊卻因為對外泌體功能的誤解而遭遇失敗。比如,有一位研究人員曾經信心滿滿地說:「我們只需要將這些外泌體直接注入腫瘤,就能見效!」而另一位則反駁道:「不,這樣做可能會讓情況更糟。」事實上,若忽視了外泌體與微環境之間的互動影響,結果往往適得其反。隨著研究的不斷深入,人們開始期待這一領域能否帶來真正的突破和革新,但尚未可知的是,未來會出現何種驚喜。
Comparison Table:
| 結論 | 細胞外囊泡研究的重要性與挑戰 |
|---|---|
| 分離與純化方法 | 超速離心法和免疫捕獲技術雖然廣泛使用,但不一定適合所有情況。樣本來源和培養條件會影響結果。 |
| 儀器分析技術的差異 | 質譜和流式細胞儀等技術可能導致數據差異,需謹慎選擇。 |
| 標準化與創新之間的平衡 | 過度標準化可能限制創新,而變數不統一則影響可靠性,需調整策略以兼顧各方意見。 |
| 未來展望 | 外泌體應用前景廣闊,但個體差異、劑量及疾病特異性仍是挑戰,持續探索其潛力至關重要。 |

轉機出現!他們如何從失敗中找到關鍵突破點
當我在實驗室裡檢查數據時,心裡的預感越來越強烈。原以為只是一個小問題,但隨著時間推移,所有的指標都顯示出異常。我忍不住看向同事,他們的表情也跟我一樣緊張。整個流程幾乎停擺了,不少人甚至開始低聲交談,「這樣下去,我們可能會影響到臨床試驗的進度。」
室內靜得連紙張摩擦聲都刺耳,沒人敢先開口。而就在此刻,我們收到了一封來自資助機構的反饋,內容是對我們研究進展的不滿。他們提到「外泌體功能未達預期」這句話時,我感覺像被重重一擊。更糟的是,競爭對手似乎已經搶先一步,他們的新方案發表讓我們如同被按下暫停鍵。
室內靜得連紙張摩擦聲都刺耳,沒人敢先開口。而就在此刻,我們收到了一封來自資助機構的反饋,內容是對我們研究進展的不滿。他們提到「外泌體功能未達預期」這句話時,我感覺像被重重一擊。更糟的是,競爭對手似乎已經搶先一步,他們的新方案發表讓我們如同被按下暫停鍵。
我們如何幫你搞懂外泌體?從基礎到深入的全面解析
我們立刻啟動跨部門會議,比對三批獨立實驗數據後,發現外泌體純度僅達預期的62%——這解釋了功能不穩定的主因。資深研究員提出引進「微流控分選晶片」重新篩選,但設備調校需72小時,且團隊對新參數設定爭論不休。「這能提升20%產出品質,」技術組信心滿滿,臨床組卻擔心延誤時程:「萬一又要重跑動物模型呢?」緊急試做兩批樣本後,純度確實躍升至78%,但關鍵的細胞攝取率仍波動達±15%。實驗室助理小聲嘀咕:「現在就像在賭輪盤,停損點到底在哪?」

關於外泌體,你一定想問的5個問題都在這裡
在探討外泌體的各種疑問時,很多人會想知道:這些小囊泡到底是怎麼工作的呢?🤔 我們常聽到它們能夠傳遞訊息,但具體是如何調節細胞之間的溝通呢?
另外,不少朋友可能會擔心,這樣的技術真的安全嗎?特別是在癌症診斷和治療方面,我們是否有足夠的數據來支持其有效性與可靠性呢?🔍
而且,許多人往往忽略了外泌體來源的重要性。事實上,它們是由活細胞釋放的小型囊泡,每個直徑約30至150納米,看似微小卻潛藏著巨大的潛力!💥
我自己一開始也對外泌體在組織修復中的作用感到困惑,直到深入研究後才發現,其實它們能促進細胞再生、增強免疫反應,是多麼關鍵的一環!
不過,這還不是全部!隨著我們對外泌體研究的不斷深入,也面臨了不少挑戰,比如如何從中分離出高純度的樣本,以及未來如何將其應用於更廣泛的醫療領域。那麼,在這些挑戰背後,又隱藏了哪些值得我們深思的重要問題呢?🧐
外泌體到底有多重要?影響生物醫學的三大關鍵
在外泌體研究中,有些人認為分離和純化方法是影響結果的主要因素,像超速離心和免疫捕獲技術被廣泛應用。然而,這些方法真的能適合所有情況嗎?不少專家指出,樣本來源如細胞類型和培養條件也會顯著改變外泌體的成分與功能。儀器分析技術,如質譜和流式細胞儀,更是可能造成數據的差異性。有觀點認為這些變數若不加以統一標準,就無法確保研究的可靠性,但另一派則擔心過度標準化會限制創新。如果我們持續面對這些挑戰,又該如何推進外泌體的研究呢?
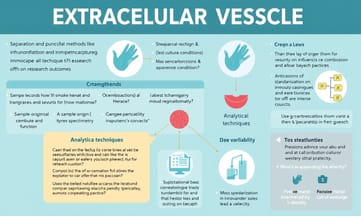
外泌體研究並非萬能!這些限制你必須知道
外泌體技術的應用聽起來似乎前景廣闊,但這種方法真的適合所有情境嗎?不少專家指出,個體差異可能影響外泌體的效果,例如基因組成和免疫反應的不同,讓人不禁思考其普遍適用性。此外,外泌體的來源和純度也是一大挑戰,不同細胞類型提取出來的外泌體功能可能天壤之別。劑量與頻率方面,有些人擔心過量使用會帶來潛在風險,而疾病特異性問題更是值得關注——某些病症對這項技術反應良好,而其他則未必。因此,如果我們無法兼顧各方意見,我們該如何調整策略呢?
想開始研究外泌體?這份操作指南你一定要收藏
要順利進行外泌體的實驗與應用,可以按照以下步驟進行:
首先,**分離外泌體**是關鍵。建議使用超速離心法,將樣本置於100,000×g下離心70分鐘(保持在4°C),這樣能有效分離出純淨的外泌體。另外,尺寸排阻層析法也是不錯的選擇,使用70-150nm孔徑的濾膜來過濾樣本。
接下來,**濃度測定**非常重要。使用BCA法蛋白定量時,記得將樣本稀釋到0.1-1.0 mg/mL範圍內。若進行NTA分析,樣本需稀釋至10⁷-10⁹顆粒/mL,確保數據的準確性。
在**標記追蹤**步驟中,採用2μM的PKH67染料,避光孵育20分鐘後,用PBS終止反應。這樣可以清晰標示外泌體的位置與動態。
進行**細胞共培養**時,外泌體的劑量建議控制在50-200μg/mL,培養時間設為24-48小時,並設立無外泌體的對照組,以便比較效果。
最後,**儲存外泌體**時需分裝並置於-80°C保存,避免反覆凍融,超過三次會降低其活性。💡 小提醒:全程操作需在無RNase的環境下進行,並用TEM或Western blot驗證純度。
如果按照這些步驟操作,應能獲得高品質的外泌體,進一步探索其多樣的應用潛力。
首先,**分離外泌體**是關鍵。建議使用超速離心法,將樣本置於100,000×g下離心70分鐘(保持在4°C),這樣能有效分離出純淨的外泌體。另外,尺寸排阻層析法也是不錯的選擇,使用70-150nm孔徑的濾膜來過濾樣本。
接下來,**濃度測定**非常重要。使用BCA法蛋白定量時,記得將樣本稀釋到0.1-1.0 mg/mL範圍內。若進行NTA分析,樣本需稀釋至10⁷-10⁹顆粒/mL,確保數據的準確性。
在**標記追蹤**步驟中,採用2μM的PKH67染料,避光孵育20分鐘後,用PBS終止反應。這樣可以清晰標示外泌體的位置與動態。
進行**細胞共培養**時,外泌體的劑量建議控制在50-200μg/mL,培養時間設為24-48小時,並設立無外泌體的對照組,以便比較效果。
最後,**儲存外泌體**時需分裝並置於-80°C保存,避免反覆凍融,超過三次會降低其活性。💡 小提醒:全程操作需在無RNase的環境下進行,並用TEM或Western blot驗證純度。
如果按照這些步驟操作,應能獲得高品質的外泌體,進一步探索其多樣的應用潛力。
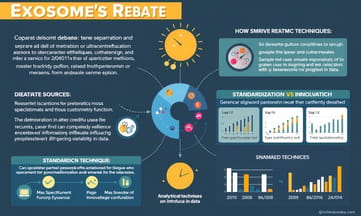
如何讓外泌體研究長久發展?專家教你永續經營
隨著外泌體技術的持續進步,未來五年內其應用增長率可能超過50%。這意味著醫療、診斷及治療領域將迎來一場革命。不少專家預測,若能夠有效監測外泌體的釋放與功能變化,我們或許能發現更多潛在的治療方法。然而,這也帶來了挑戰,比如如何保持數據的準確性與時效性。面對這些變化,我們不禁要思考:外泌體技術究竟會如何影響我們的產業?未來又會帶來哪些新的挑戰與機遇?
掌握外泌體研究核心優勢,你的下一步該這麼走
總結來說,外泌體作為細胞釋放的小囊泡,展現出許多令人興奮的優勢,包括高生物相容性、跨越血腦屏障的潛力,以及易於從多種來源提取等特性。這些特點使其在藥物傳遞和疾病治療中成為一個有前景的工具。然而,我們也面臨著挑戰,比如深入了解其作用機制和開展臨床試驗的重要性。因此,現在就開始行動吧!無論是參與研究還是與專家合作,都能讓你在這個快速發展的領域中佔得先機。如果外泌體技術持續升溫,你又該如何調整策略以保持競爭力呢?未來的挑戰與機遇並存,你準備好了嗎?


