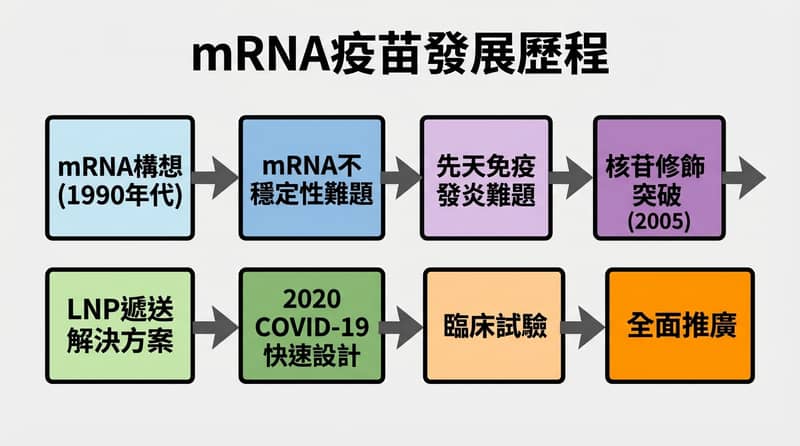
2020 年底,mRNA COVID-19 疫苗在大型臨床試驗中公布的保護力數字,像 Pfizer-BioNTech(BNT162b2)約 95%、Moderna(mRNA-1273)約 94% 那樣,直接把「mRNA 只是理論玩具」的說法打到牆上。這件事的核心不是一夜爆紅,而是 Katalin Karikó 和 Drew Weissman 在 2005 年做出「核苷修飾 mRNA 降低先天免疫反應」的關鍵發現,讓 mRNA 能進人體而不先把警報拉爆。
- 關鍵人:Katalin Karikó、Drew Weissman
- 關鍵技術詞:nucleoside-modified mRNA、lipid nanoparticles(LNP)
- 關鍵難題:mRNA 太脆、免疫系統會先發炎、怎麼送進細胞
- 關鍵轉折:COVID-19 逼大家把「做得出來」變成「做得夠快」
- 你要記得的那句:mRNA 疫苗是平台,不是只為了 COVID-19
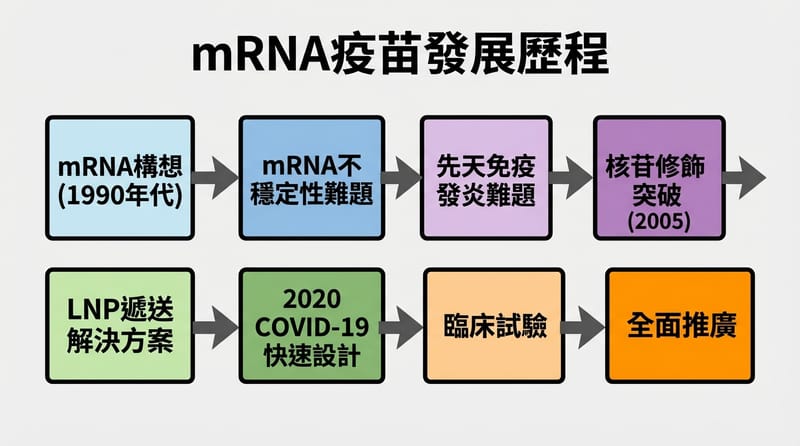
先破案:mRNA 為什麼以前一直做不成
mRNA 疫苗早期卡關的主因是「分子本體太容易壞」加上「先天免疫把它當入侵者」,所以就算把 mRNA 打進去,也常在到達細胞前分解,或先引發發炎反應而不是產生想要的蛋白。解法最後變成兩條線:改 mRNA 的化學細節、再用 LNP 把它包起來送到細胞。
偵探視角:你有沒有發現,這案子根本不是「mRNA 能不能指揮細胞做蛋白」——那個大家 70 年代就知道了;真正的兇手是「你還沒開口講話就被門口保全趕出去」。
mRNA 本身很脆,遇到環境裡的核酸酶(RNase)就像遇到碎紙機。咻。沒了。
更麻煩的是免疫系統。身體看到外來 RNA,會啟動先天免疫反應(你可以把它想成警鈴+消防灑水系統一起開),結果你想要的是「教會身體認得目標蛋白」,它卻先把場子弄得一團糟。
講到「灑水系統」,我突然想到很多人以為發燒就是疫苗在「發功」——欸不一定,發燒只是免疫反應的一種表現,跟你想要的免疫記憶是不是有好好建立,兩者不是同一條線。
好,拉回來。總之早期就是:脆+吵。
關鍵突破:Karikó 和 Weissman 到底改了什麼
Katalin Karikó 與 Drew Weissman 的核心貢獻是證明「把 mRNA 的某些核苷做修飾(nucleoside modification)」可以降低先天免疫系統的警報反應,同時讓 mRNA 更能在細胞裡順利被翻譯成蛋白。這讓 mRNA 從「一打進去就被當垃圾」變成「能安靜工作一段時間」的工具。
故事味但不灑狗血:原文那段我看了其實有點…嗯,像電影預告。可現實更冷:研究經費被打槍、升等卡住、同行翻白眼。這種東西比失戀還磨人,因為你連「我到底哪裡做錯」都很難被告知。
Karikó 的堅持點很單純:mRNA 不是怪力亂神,它只是個「訊息」。如果訊息能送到、能被讀到,很多病(感染、某些癌症免疫治療)就有新路。
然後她跟 Weissman 做的不是「突然靈光乍現」,而是一堆失敗、再一堆失敗、再…你知道的,反正研究室那種日常,數據一看就想去買鹽酥雞壓壓驚。
技術小抓手:你可以記「核苷修飾」這四個字就好,細節要講會很化學,但方向就是:讓 mRNA 看起來沒那麼像「外來入侵訊號」,免疫系統就不會先把它打爆。
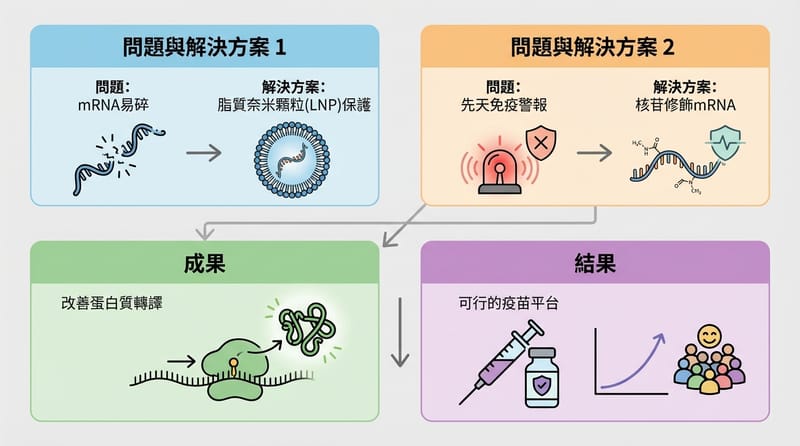
COVID-19 那一年:為什麼 mRNA 變成「能跑的方案」
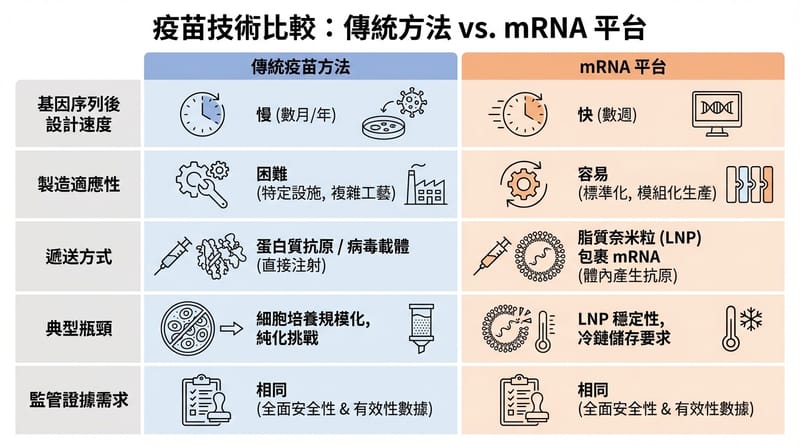
COVID-19 之所以讓 mRNA 疫苗被推到舞台中央,是因為 mRNA 平台的設計速度可以跟上病毒基因序列的公布節奏:拿到序列、選定目標蛋白(例如 SARS-CoV-2 的 spike)、設計對應 mRNA,再進入製造與試驗流程。相較傳統疫苗路線,mRNA 的「改配方」速度明顯更快,但仍需要臨床試驗與監管審查來確認安全與效力。
那種「時間不夠」的壓力:我記得那時候的氛圍就是,新聞每天在跳數字,醫院像被海浪拍打——欸我不講抽象,講具體:病床、氧氣、護理人力,全部都是硬上限。你再慢,代價就不是「市場被搶走」,是人真的會不見。
所以各路人馬開始合作:學界、公司、政府單位、監管機構。原文講得很熱血,我換個說法:錢跟流程突然能動了。
但別誤會,這不是「隨便快轉」。監管快,是因為資料一批一批送、一批一批看;你不交資料也沒人會憑空放你過。
另外一個關鍵詞:LNP(lipid nanoparticles)。mRNA 不是自己游進細胞的,它需要「載具」。LNP 就像把訊息塞進一顆很小的油脂泡泡,讓它比較有機會穿過細胞膜。
講到油脂泡泡,我突然想到很多人看到「脂質」就先怕胖。拜託,這不是你喝的珍奶奶蓋,這是藥物遞送系統,量級跟用途完全不同。
三個常見迷思,快問快答直接拆
規則:下面 3 題我用「一句直球+一個可操作的檢查點」回你,少囉嗦。
迷思 1:mRNA 疫苗會改變我的 DNA 嗎?mRNA 疫苗的 mRNA 不需要進入細胞核,也不會整合進 DNA;它主要在細胞質被翻譯成蛋白,之後 mRNA 會被分解。檢查點:你去看「細胞核(nucleus)」「reverse transcriptase」「genome integration」這些詞在官方科普裡怎麼被解釋,沒有這些機制就不會發生「寫進 DNA」那件事。
迷思 2:發燒越高=免疫越強嗎?發燒只是免疫反應的一種表現,並不能當作保護力的量尺;保護力要看臨床試驗的感染率差異、重症與住院的降低幅度。檢查點:看疫苗的臨床試驗報告怎麼定義 endpoint(例如有症狀感染、重症、住院),不要用體感當指標。
迷思 3:mRNA 太新了所以一定很危險?mRNA 作為概念不新,真正成熟是因為核苷修飾與 LNP 等關鍵技術逐步到位,安全性仍要靠分期臨床試驗與上市後監測累積證據。檢查點:你可以查「pharmacovigilance(藥物安全監測)」或各國不良事件通報系統的運作方式,看看它怎麼收資料、怎麼判讀,而不是只看截圖。
我覺得最詭異的點:這故事其實在講資源怎麼分
mRNA 疫苗的成功故事,同時也是「長期基礎研究」如何在關鍵時刻變成公共衛生工具的案例;Karikó 的核苷修飾研究、LNP 遞送技術、以及後續公司與學界的工程化整合,都是多年累積才在 COVID-19 被一次用到極限。這提醒大家:投資基礎研究不是做慈善,是在幫未來的危機準備可用的工具箱。
低能量碎念:我其實很怕那種「成功學版本」的敘事:好像只要夠努力就會被看見。現實常常是,你努力了很久,還是沒人理你;直到某個大事件來了,大家突然說「哇你怎麼那麼早就想到」。
嗯,對,就是那種遲到的掌聲。聽起來很浪漫,其實很冷。
而且原文也有提到:就算做出來了,推廣也不是童話。供應鏈、冷鏈、施打動線、民眾猶豫…每一個都能把你拖慢。你看過疫苗在診所冰箱裡的擺法嗎?那不是「科學」兩個字就能解決,是物流+人力+制度的拼裝。
講到制度,在台灣這種事最後一定會扯到一堆單位:衛福部、食藥署(TFDA)、疾管署(CDC)。有人覺得煩,我懂,但如果沒有這些流程,大家又會反過來問「誰幫我把關」。就是這樣,兩面都有人罵。
下一步會去哪:mRNA 不只拿來打 COVID-19
mRNA 技術的長期方向通常被視為「可快速換目標的醫療平台」,包含新型傳染病疫苗、某些癌症的個人化免疫療法,以及其他需要讓身體短期表達特定蛋白的應用。這些應用仍需要針對不同疾病做臨床驗證、劑量與遞送設計,不是把 COVID-19 的配方換名字就能直接套用。
你可能會想像的畫面:像疊樂高一樣,今天換成對付流感,明天換成對付某個寄生蟲。可以想像,但別把它想得太簡單,因為每個疾病的免疫逃脫方式不同,人體也不是同一個地形。
但我承認,平台感這件事真的很…怎麼講,會讓人想多看兩眼。對,就是那種「欸這玩意兒以後可能很常出現」的感覺。
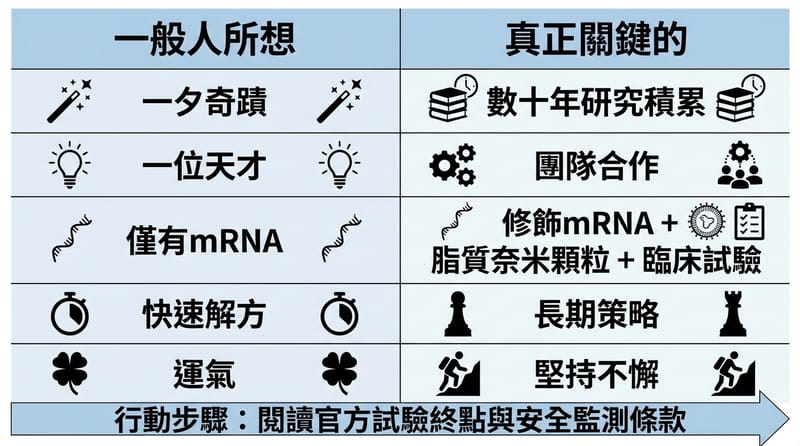
核心金句:mRNA 疫苗不是突然從天上掉下來的,它是「核苷修飾 mRNA+LNP 遞送+臨床試驗證據」這三件事慢慢湊齊,才在 COVID-19 被推上前線的。
純分享收尾:如果你想找一個不會被短影音帶節奏的入口,去翻「TFDA 疫苗審查」這個關鍵字,順便把「藥物安全監測 pharmacovigilance」一起丟進去查,會看到很多你以為沒人在管、其實有人在管的細節。